식품의약품안전처(처장 오유경)는 2020년 코로나19 발생 초기 응급환자에 대한 코로나19 검사 소요시간 단축(1시간 이내)을 위해 ‘긴급사용승인*’한 ‘코로나19 응급용 유전자진단시약**’ 9개 제품의 긴급사용을 6월 1일자로 종료하며, 6월 2일부터는 정식허가 제품만 코로나19 검사에 사용할 것을 당부했습니다.
* 코로나19 팬데믹 등 공중보건 위기상황 대응을 위해 허가받지 않은 제품을 한시적으로 제조·수입·판매·사용할 수 있게 하는 제도
** 응급환자 대상으로 신속하게 코로나19 감염을 확인하기 위해 1시간 이내 결과 확인이 가능한 유전자검사 제품
다만 의료기관에서 기존 제품의 재고를 소진하고, 다른 제품에 대한 도입을 준비하며 의료기관의 검사 역량과 정확도를 유지하기 위해 3개월의 유예기한을 둡니다.
이번 조치는 ‘코로나19 위기단계 하향(심각→경계) 조정 및 방역 조치 전환’(6.1.)을 대비해 ▲9개 제품 업체 간담회 ▲사용기관과 업무협의 ▲허가현황 ▲생산량·공급량·재고량 등을 종합적으로 고려한 결과, 정식허가된 응급용 21개 제품이 긴급사용승인 제품을 충분히 대체할 수 있다는 판단에 따른 것입니다.
식약처는 앞으로도 체외진단의료기기 업계와 질병관리청 등 유관기관과 긴밀한 협조를 유지해 공중보건 위기상황 시 신속하게 대응할 수 있도록 최선을 다하고 국민 안전을 지키는 기관의 역할을 충실히 수행하겠습니다.
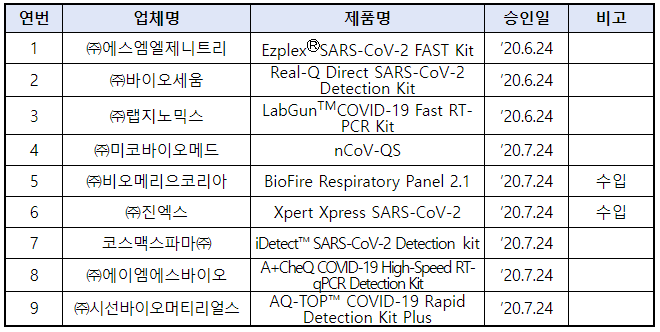
❍ 응급용 긴급사용승인 제품
출처 - 식약처
'기타정보' 카테고리의 다른 글
| 삼성전자, ‘비스포크 무풍에어컨 핏홈’ 출시 (0) | 2023.06.12 |
|---|---|
| 2022 부산해양산업조사 결과 공표 (0) | 2023.06.06 |
| 2023년 원마운트 워터파크 5월 클린데이 안내 (0) | 2023.05.23 |
| 대한항공, 넷마블에프앤씨와 전략적 파트너십 MOU 체결 (0) | 2023.05.21 |
| 2022년 아이오바이오 평균연봉 (0) | 2023.05.07 |




댓글